



CIRCULAR CONJUNTA EXTERNA 61 DE 2015
(diciembre 24)
Diario Oficial No. 49.739 de 28 de diciembre de 2015
MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL
INSTITUTO NACIONAL DE SALUD
1000-
Bogotá, 24 de diciembre de 2015
| PARA: | GOBERNADORES, ALCALDES, SECRETARÍAS DISTRITALES, MUNICIPALES Y DEPARTAMENTALES DE SALUD, COORDINADORES DE VIGILANCIA EN SALUD PÚBLICA, COORDINADORES DEL PROGRAMA DE ENFERMEDADES TRANSMITIDAS POR VECTORES ETV, ENTIDADES ADMINISTRADORAS DE PLANES DE BENEFICIOS, RESPONSABLES DE REGÍMENES ESPECIALES Y DE EXCEPCIÓN, INSTITUCIONES PRESTADORAS DE SERVICIOS DE SALUD, LABORATORIOS DISTRITALES Y DEPARTAMENTALES DE SALUD PÚBLICA, LABORATORIOS CLÍNICOS Y SERVICIOS DE ATENCIÓN MÉDICA EN PUNTOS DE ENTRADA INTERNACIONALES. |
| DE: | MINISTERIO DE SALUD Y PROTECCIÓN SOCIAL INSTITUTO NACIONAL DE SALUD |
| ASUNTO: | Vigilancia de la fiebre por virus Zika (ZIKV) en su fase II epidémica y fortalecimiento de la prevención de la fiebre por virus Zika en grupos de riesgo. |
En octubre de 2015, fue publicada la circular externa 043 de 2015 para orientar la vigilancia, prevención y control ante la introducción del virus Zika en Colombia.
Considerando que al momento de emisión de la presente circular, el virus se encuentra circulando en 28 entidades territoriales y 150 municipios, se informa el inicio de la fase expansiva o epidémica, motivo por el cual mediante esta circular conjunta, el Ministerio de Salud y Protección Social y el Instituto Nacional de Salud, actualizan elementos básicos de la vigilancia en salud pública como son las definiciones de caso, las estrategias de vigilancia a utilizar, el seguimiento de las posibles complicaciones y el análisis de la mortalidad.
En los 951 municipios y centros poblados cuya cabecera están entre 0 y 2.200 msnm, se encuentran dos escenarios que se definen así (ver Tabla No 1):
1. Con transmisión: municipios y centros poblados que ya tengan casos confirmados por laboratorio y se encuentren entre 0 y 2200 msnm.
2. Sin transmisión: municipios y centros poblados ubicados por debajo de 2.200 msnm, con condiciones para la presencia de vectores del género Aedes y que no tengan casos confirmados por laboratorio.
Tabla No 1. Escenarios epidemiológicos y tipo de población para la detección de la circulación del ZIKV, y confirmación de casos por laboratorio
| Escenarios epidemiológicos y tipo de población | Muestra de suero | Ingreso al SIVIGILA como: | Según resultados de laboratorio queda: |
| Grupo de riesgo* en municipio con o sin trasmisión | Sí | Sospechoso | Confirmado o descartado |
| Población general procedente del extranjero | Sí | Sospechoso | Confirmado o descartado |
| Población general municipios con transmisión | No | Confirmado por clínica | No aplica |
| Población en municipios sin transmisión (con aedes) | Sí** | Sospechoso | Confirmado o descartado |
*Grupos de riesgo: gestantes, neonatos, menores de un año, mayores de 65 años y personas con co-morbilidades.
**Número de muestras: Según metodología establecida por el MSPS e INS (DVARSP, LNR Virología).
Debido a los recientes hallazgos en Brasil[1] en los cuales se describe la posible relación temporo-espacial de la enfermedad por virus Zika con la presentación de anomalías congénitas y la posible presentación de alteraciones neurológicas y virus Zika, se emitieron los lineamientos operativos de vigilancia desde el Instituto nacional de Salud mediante la Circular 063 de 15 diciembre de 2015 sobre Intensificación de Vigilancia en salud pública de defectos congénitos y muertes perinatales y Circular 064 del 15 de diciembre de 2015 sobre Vigilancia y notificación de los Síndromes neurológicos con sospecha previa o confirmación de enfermedad por virus Zika, las cuales deben ser socializadas en los servicios de salud.
1. Definiciones de caso, enfermedad por ZIKV
1.1 Definición de caso
| TIPO DE CASO | CARACTERÍSTICAS DE LA CLASIFICACIÓN |
| Caso sospechoso | Grupo a riesgo (neonatos, menores de 1 año, gestantes, personas con 65 años y más y/o con co-morbilidades): persona que presente exantema y elevación de la temperatura corporal axilar mayor de 37,2 grados centígrados y uno o más de los siguientes síntomas que no se explican por otras condiciones médicas: conjuntivitis no purulenta o hiperemia conjuntival, artralgias, mialgias, cefalea o malestar general; y que haya estado en lugares a menos de 2200 msnm, y/o en países con o sin circulación confirmada de este virus. Estas personas ameritan la toma de muestra de suero en los tiempos establecidos para confirmación o descarte por laboratorio del virus Zika sin excepción. |
| Población general procedente del extranjero: persona que presente exantema y elevación de la temperatura corporal axilar mayor de 37,2 grados centígrados y uno o más de los siguientes síntomas que no se explican por otras condiciones médicas: conjuntivitis no purulenta o hiperemia conjuntival, artralgias o mialgias y cefalea o malestar general y que haya estado en lugares a menos de 2200 msnm, y/o en países con o sin circulación confirmada de este virus. Estas personas ameritan la toma de muestra de suero para confirmación por laboratorio del virus Zika sin excepción. | |
| Población general procedente de municipios sin transmisión de ZIKV confirmada: persona que presente exantema y elevación de la temperatura corporal axilar mayor de 37,2 grados centígrados y uno o más de los siguientes síntomas que no se explican por otras condiciones médicas: conjuntivitis no purulenta o hiperemia conjuntival, prurito, artralgias, mialgias, cefalea o malestar general, y que haya estado en lugares a menos de 2200 msnm. Se tomarán muestras para confirmación diagnóstica según cálculo de muestra en áreas sin confirmación de circulación viral. | |
| Caso confirmado por clínica | Población general procedente de municipios con transmisión de ZIKV confirmada: Persona que haya estado en los últimos 15 días antes del inicio de síntomas en lugares a menos de 2200 msnm, con confirmación de circulación autóctona del virus Zika, y que presente exantema y elevación de la temperatura corporal axilar mayor de 37,2 grados centígrados y uno o más de los siguientes síntomas que no se explican por otras condiciones médicas: conjuntivitis no purulenta o hiperemia conjuntival, prurito, artralgias, mialgias, cefalea o malestar general. |
| Caso confirmado por laboratorio | Caso sospechoso con resultado positivo para ZIKV mediante RT-PCR ZIKV, realizada en el Laboratorio Nacional de Referencia de Virología de la Red Nacional de Laboratorios del Instituto Nacional de Salud, o centros colaboradores designados por el INS (ver algoritmo diagnóstico). |
| Caso descartado | Caso sospechoso al que se le tomó muestra para laboratorio dentro de los tiempos establecidos para la detección del virus, y presentó resultados negativos para ZIKV (ver algoritmo diagnóstico). |
Una vez se identifique circulación viral en un número de casos predefinido por municipio, no será necesario tomar muestras de suero adicionales en población general, y los casos ingresarán al sistema de vigilancia epidemiológica como confirmados por clínica. Se exceptúan los grupos de riesgo.
1.2. Muerte posiblemente asociada a ZIKV
| TIPO DE CASO | CARACTERÍSTICAS DE LA CLASIFICACIÓN |
| Caso sospechoso de muerte | Toda persona que fallece y cumple con alguna de las definiciones de caso de enfermedad por ZIKV (caso sospechoso, caso confirmado por clínica o caso confirmado por laboratorio). Este caso amerita obligatoriamente la toma de muestra de tejidos para estudios histopatológicos y virológicos (ver numeral 3.1.1 –Recolección-). |
| Caso confirmado | Caso sospechoso de muerte a quien por métodos de laboratorio se le confirma la presencia del ZIKV y/o hallazgos histopatológicos compatibles con lesiones por Arbovirus, y que mediante la realización de una unidad de análisis por el nivel Nacional (Ministerio de Salud y Protección Social e INS), se concluye que la enfermedad por ZIKV fue la causa básica de la muerte. |
| Caso descartado | Caso sospechoso de muerte a quien por métodos de laboratorio se le descarta la presencia del virus y/o hallazgos histopatológicos compatibles con la infección por el virus, y que mediante la realización de una unidad de análisis por el nivel Nacional (Ministerio de Salud y Protección Social e INS), se concluye que el ZIKV no fue la causa básica de la muerte. Este caso deberá ser ajustado en el Sivigila como clasificación final descartado. |
2. Notificación del evento enfermedad por el virus ZIKV al sistema de vigilancia epidemiológica
2.1. Sivigila: Durante la fase de introducción del virus, las UPGD realizarán la notificación individual de todos los casos sospechosos y confirmados, de infección por el virus ZIKV través de la ficha de datos básicos con el código 895.
Es necesario que cuando se notifiquen casos en mujeres gestantes se diligencie en la ficha de datos básicos la variable 2.20 Grupo poblacional: gestante. Lo anterior para garantizar que se identifiquen las pacientes y poder realimentar a las EAPB a través del Sivigila web.
Las EAPB deberán revisar el Sivigila web, para verificar las gestantes que han sido notificadas bajo el código 895, con el fin de identificar sus afiliadas y garantizar el seguimiento clínico estricto durante el embarazo. Esta información se actualiza de forma semanal pero puede ser consultada en cualquier momento.
Es responsabilidad de las EAPB el seguimiento de las gestantes con sospecha o confirmación de enfermedad por virus Zika, en cumplimiento de la Resolución 412 del año 2000 y las acciones específicas del control prenatal, teniendo en cuenta que la infección por el virus ZIKV en el embarazo se trata de un evento de interés en salud pública y que frente a esta situación el embarazo se considera de alto riesgo. Por tanto se deberá garantizar a la gestante el seguimiento ecográfico y la toma de muestra de líquido amniótico cuando lo solicite el médico tratante. La muestra de líquido amniótico deberá ser enviada al Laboratorio de Salud Pública de la entidad territorial correspondiente para diagnóstico de virus Zika.
2.2. Reporte de Información Complementaria para el seguimiento de las Gestantes. De manera continua las EAPB deberán cargar la información relacionada con estas gestantes, de las variables no contenidas en la Ficha de datos básicos 895, a través de la plataforma PISIS, que estará disponible en el anexo y en las fechas y periodos que defina el Ministerio de Salud y Protección Social.
2.3. Búsquedas Activas Institucionales: Para facilitar la Búsqueda Activa Institucional basada en los Registros Individuales de Prestación de Servicios RIPS, se hace pertinente verificar el uso adecuado de los códigos de la Clasificación Internacional de Enfermedades CIE10, debido a que por instrucciones del Equipo de Vigilancia Global de OMS, se hará efectiva la introducción de los nuevos códigos CIE10 para la Enfermedad por virus ZIKA y sus sinónimos (Fiebre por virus Zika; Infección por el virus Zika; Encefalitis Zika), en reemplazo del código A92.8 Otras fiebres especificadas transmitidas por mosquitos, así:
U06 para Enfermedad por virus Zika (Zika virus disease) codificación a 3 caracteres.
U06.9 para Enfermedad por virus Zika, no especificado (Zika virus disease, unspecified) codificación a 4 caracteres.
3. Orientaciones para la confirmación por laboratorio (ver Tabla No 2).
Tabla No 2. Criterios para toma de muestra según población afectada y escenario epidemiológico.
| AGENTE ETIOLÓGICO | CONDICIÓN | TOTAL DE MUESTRAS |
| Virus Zika | Personas en grupos de riesgo* | Todos los casos |
| Población general en municipios sin transmisión | Cálculo del número de muestras a enviar | |
| Población general procedente del extranjero. | Todos los casos | |
| Muerte | Todos los casos | |
*Grupos de riesgo: gestantes, neonatos, menores de un año, mayores de 65 años y personas con co-morbilidades.
Respecto al número de muestras que se tomarán en población general en municipios sin transmisión confirmada por laboratorio, esta información se enviará a los referentes de vigilancia y de los LDSP de todo el país (ver anexo, metodología establecida por el MSPS e INS).
3.1. Recolección y envío de muestras (suero o tejidos) para identificación de ZIKV y otros agentes etiológicos, y reporte de resultados.
3.1.1. Recolección
La recolección de muestras en personas vivas debe realizarse en aquellas que cumplan con la definición de caso sospechoso con un periodo máximo de evolución de cinco días posterior al inicio de síntomas.
Una vez fallezca la persona, se deberá tomar doble muestra de los siguientes órganos: hígado, bazo, riñón, miocardio, pulmón, cerebro, médula ósea, ganglio linfático; una muestra deberá ser refrigerada en solución salina para estudios virológicos y la otra en solución fijadora de formol al 10 % pH neutro para estudios histopatológicos. Ante mortalidad materna, fetal, perinatal e infantil, se remiten las mismas muestras y según corresponda, fragmento de placenta y timo. Si el deceso fue precedido de manifestaciones neurológicas de polineuropatía ascendente aguda o subaguda semejante a Síndrome de Guillain Barré, remitir además de lo anterior, cortes representativos de las raíces de nervios dorsales lo más proximal a la médula espinal en sus diferentes localizaciones (cervical, torácica y lumbar). Ver Decreto 786 de 1990.
3.1.2. Manejo y remisión de muestras
Las muestras de suero deben ser almacenadas en condiciones de congelación (-10 a -20oC) y enviadas al Laboratorio de Salud Pública Departamental dentro de las primeras 48 horas después de su recolección. A su vez, el Laboratorio de Salud Pública debe garantizar las mismas condiciones de almacenamiento y transporte para remitir al Laboratorio de Virología del Instituto Nacional de Salud.
La documentación que acompaña la muestra debe ser remitida por la IPS en donde se detectó el caso sospechoso y consta de: ficha epidemiológica de datos básicos donde se evidencie la fecha de inicio de síntomas y el antecedente de viaje, ficha de laboratorio donde se evidencie la fecha de recolección de la muestra y un resumen de historia clínica.
Estas muestras deberán ser remitidas al Laboratorio de Salud Pública con la documentación respectiva: ficha epidemiológica de datos básicos código 217, ficha de laboratorio con todos los campos diligenciados (fecha de inicio de síntomas y fecha de recolección de la muestra) e historia clínica.
El Laboratorio de Salud Pública verificará las condiciones en que lleguen las muestras y que estén acompañadas de la documentación ya definida. Remitirá las muestras al Laboratorio de Virología del INS.
La recolección, almacenamiento y transporte adecuado, son aspectos fundamentales para realizar un diagnóstico confiable de ZIKV. El Instituto Nacional de Salud se reservará la decisión de procesar o no las muestras que no cumplan con las características descritas que permitan la detección del virus.
3.1.3. Reporte de resultados
La emisión de los reportes de resultados, se realizará conforme al flujo establecido dentro de los procesos del Laboratorio Nacional de Referencia del Instituto Nacional de Salud. Se solicita que los Laboratorios de Salud Pública reporten en forma inmediata a las unidades de epidemiología e IPS, los resultados emitidos por el Laboratorio Nacional de Referencia (ver Anexo No 1).
3.2. Algoritmo del Laboratorio Nacional de Referencia (LNR) para identificación virológica del ZIKV
Considerando la difícil identificación del ZIKV desde el punto de vista clínico por las manifestaciones semejantes a las que presentan otros virus como sarampión, rubeola, dengue y chikungunya, el Laboratorio de Virología del Instituto Nacional de Salud ha definido dos estrategias de búsqueda en muestras procedentes de pacientes que hayan ingresado como casos sospechosos de estas enfermedades con el fin de incrementar la probabilidad de identificarlo (ver Anexo No 2).
Estrategia 1. Vigilancia rutinaria de Arbovirus.
Esta vigilancia se realizará a la población general teniendo en cuenta el evento notificado en la ficha epidemiológica (dengue, Chikungunya y zika), la confirmación de la circulación del evento y epidemiología en la zona geográfica; específicamente para Zika se tendrá en cuenta un diseño estadístico el cual establecerá el número máximo de muestras requeridas para confirmar la circulación en el municipio.
Estrategia 2. Vigilancia en Grupos de Riesgo y mortalidades
Se realizarán todas las pruebas disponibles en el laboratorio de Arbovirus a la población de riesgo (menores de un año, gestantes, mayores de 65 años, co-morbilidades, y a las mortalidades independiente del evento notificado.
4. Análisis de la información y orientación de la acción
Durante la fase epidémica, la información deberá ser analizada semanalmente por los servicios de epidemiología para que el programa de ETV a nivel municipal, departamental y nacional oriente las acciones de promoción de la salud, prevención, atención de pacientes y gestión de contingencias. Este análisis deberá permitir a los municipios, focalizar las acciones a nivel de barrio y a los departamentos a nivel del municipio, además de identificar con oportunidad cualquier cambio en los patrones de la enfermedad.
5. Difusión de la información
A nivel nacional la información oficial se continuará publicando con un nivel de desagregación municipal en el BES (Boletín Epidemiológico Semanal: http://www.ins.gov.co/boletin-epidemiologico/Paginas/default.aspx), el cual se puede consultar en la página electrónica del Instituto Nacional de Salud. Cada entidad territorial deberá enlazarse a esta publicación en forma electrónica a través de sus páginas web institucionales.
Para obtener más información sobre características del ZIKV y las alertas que se publiquen a nivel regional, se recomienda consultar las páginas de la Organización Panamericana de la Salud (http://www.paho.org/hq/), el Centro de Control de Enfermedades de Atlanta http://www.cdc.gov/), y el Centro Nacional de Enlace Colombia. https://www.minsalud.gov.co/salud/publica/CNE/Paginas/alertas-internacionales-2.aspx
En caso de que requieran realizar alguna consulta o notificar alguna situación de interés epidemiológico relacionada con la enfermedad por ZIKV en las entidades territoriales; por favor comunicarse a los siguientes teléfonos o correos electrónicos:
| NOMBRE | ENTIDAD - ÁREA | CORREOS ELECTRÓNICOS | TELÉFONO |
| Jacqueline Espinosa – Pilar Zambrano | Ministerio de Salud y Protección Social – CNE – GVSP - Dirección de Epidemiología y Demografía | cne@minsalud.gov.co, jespinosam@minsalud.gov.co, czambrano@minsalud.gov.co | 3305000 – Ext. 3758, 3722, 3744 |
| Julio Padilla - Fernando Galindo | Ministerio de Salud y Protección Social – Grupo ETV | jpadilla@minsalud.gov.co | 3305000 – Ext. 1459 |
| Natalia Tolosa - Sara Gómez | Instituto Nacional de Salud – Vigilancia ETV | etolosa@ins.gov.co sgomez@ins.gov.co | 2207700 – Ext. 1403 |
| Lissethe Pardo - Andrés Páez | Instituto Nacional de Salud – Red Nacional de Laboratorios | lpardo@ins.gov.co apaezm@ins.gov.co | 2207700 – Ext. 1425 |
Publíquese y cúmplase.
24 de diciembre de 2015.
El Ministro de Salud y Protección Social,
ALEJANDRO GAVIRIA URIBE.
La Directora (E) Instituto Nacional de Salud,
MARTHA LUCÍA OSPINA MARTÍNEZ.
FLUJOGRAMA PARA LA CLASIFICACIÓN DEL PACIENTE, NOTIFICACIÓN Y ENVÍO DE MUESTRAS AL INS PARA LA IDENTIFICACIÓN DE ZIKV.
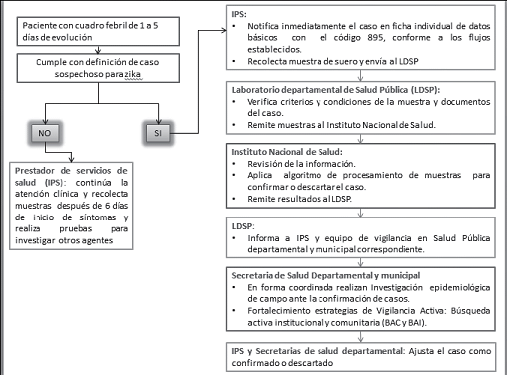
Fuente: Laboratorio Nacional de Referencia de Virología. DRSP. INS
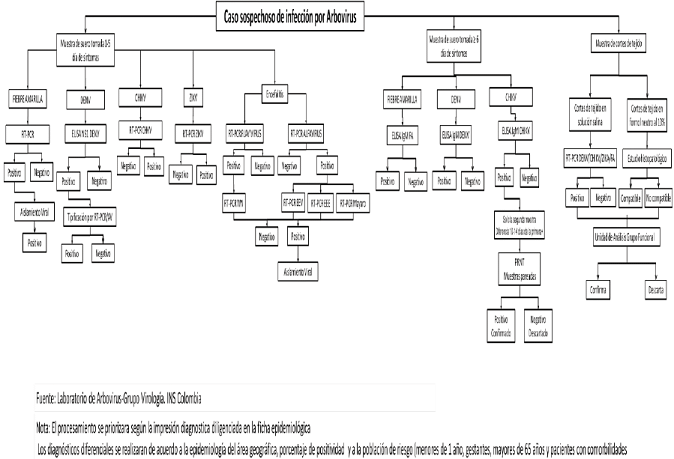
ALGORITMO PARA IDENTIFICACIÓN VIROLÓGICA DEL VIRUS ZIKA.
Fuente: Laboratorio Nacional de Referencia de Virología. DRSP. INS
* * *
1. OMS-OPS. Alerta epidemiológica. Síndrome neurológico, anomalías congénitas e infección por virus Zika. Implicaciones para la salud pública en las Américas. 1o de diciembre de 2015.
Las notas de vigencia, concordancias, notas del editor, forma de presentación y disposición de la compilación están protegidas por las normas sobre derecho de autor. En relación con estos valores jurídicos agregados, se encuentra prohibido por la normativa vigente su aprovechamiento en publicaciones similares y con fines comerciales, incluidas -pero no únicamente- la copia, adaptación, transformación, reproducción, utilización y divulgación masiva, así como todo otro uso prohibido expresamente por la normativa sobre derechos de autor, que sea contrario a la normativa sobre promoción de la competencia o que requiera autorización expresa y escrita de los autores y/o de los titulares de los derechos de autor. En caso de duda o solicitud de autorización puede comunicarse al teléfono 617-0729 en Bogotá, extensión 101. El ingreso a la página supone la aceptación sobre las normas de uso de la información aquí contenida.