RESOLUCIÓN 2025010547 DE 2025
(marzo 19)
Diario Oficial No. 53.063 de 19 de marzo de 2025
Diario Oficial disponible en la web de la Imprenta Nacional de Colombia el 20 de marzo de 2025
INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS
Por la cual se adopta un Plan de Contingencia para la gestión de trámites de Registro Sanitario y trámites asociados de la Dirección de Medicamentos y Productos Biológicos del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) y se dictan otras disposiciones.
EL DIRECTOR GENERAL Y LA DIRECTORA TÉCNICA DE MEDICAMENTOS Y PRODUCTOS BIOLÓGICOS DEL INSTITUTO NACIONAL DE VIGILANCIA DE MEDICAMENTOS Y ALIMENTOS (INVIMA),
en ejercicio de sus facultades legales y en especial las conferidas en los numerales 4, 11, 16 y 22 del artículo 10 y los numerales 7, 8 y 10 del del artículo 19 del Decreto número 2078 de 2012 y
CONSIDERANDO:
Que, en virtud de lo establecido en el artículo 209 de la Constitución Política "La función administrativa está al servicio de los intereses generales y se desarrolla con fundamento en los principios de igualdad, moralidad, eficacia, economía, celeridad, imparcialidad y publicidad, mediante la descentralización, la delegación y la desconcentración de funciones. Las autoridades administrativas deben coordinar sus actuaciones para el adecuado cumplimiento de los fines del Esta do".
Que, la Ley 1751 de 2015 "Por medio de la cual se regula el derecho fundamental a la salud y se dictan otras disposiciones", en el artículo 2o establece que el derecho fundamental a la salud "comprende el acceso a los servicios de salud de manera oportuna, eficaz y con calidad para la preservación, el mejoramiento y la promoción de la salud", estableciendo en los literales b y c del artículo 5o de la misma ley como obligaciones al Estado el formular y adoptar políticas que garanticen el goce efectivo del derecho a la salud premisa fundamental de un Estado Social de Derecho. (subrayado fuera de texto).
Que, el artículo 245 de la Ley 100 de 1993 "Por la cual se crea el sistema de seguridad social integral y se dictan otras disposiciones", se crea el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima), como un establecimiento público del orden nacional, adscrito al Ministerio de Salud, con personería jurídica, patrimonio independiente y autonomía administrativa, cuyo objeto es la ejecución de las políticas en materia de vigilancia sanitaria y de control de calidad de medicamentos, productos biológicos, alimentos, bebidas, cosméticos, dispositivos y elementos médico-quirúrgicos, odontológicos, productos naturales homeopáticos y los generados por biotecnología, reactivos de diagnóstico, y otros que puedan tener impacto en la salud individual y colectiva.
Que, el artículo 3o de la Ley 489 de 1998, respecto de los principios de la función pública consagra: "La función administrativa se desarrollará conforme a los principios constitucionales, en particular los atinentes a la buena fe, igualdad, moralidad, celeridad, economía, imparcialidad, eficacia, eficiencia, participación, publicidad, responsabilidad y transparencia. Los principios anteriores se aplicarán, igualmente, en la prestación de servicios públicos, en cuanto fueren compatibles con su naturaleza y régimen" (...).
Que, el artículo 3o de la Ley 1437 de 2011, en cuanto a la aplicación de los principios en las actuaciones administrativas por parte de las autoridades, señala: "Todas las autoridades deberán interpretar y aplicar las disposiciones que regulan las actuaciones y procedimientos administrativos a la luz de los principios consagrados en la Constitución Política, en la Parte Primera de este Código y en las leyes especiales. Las actuaciones administrativas se desarrollarán, especialmente, con arreglo a los principios del debido proceso, igualdad, imparcialidad, buena fe, moralidad, participación, responsabilidad, transparencia, publicidad, coordinación, eficacia, economía y celeridad".
4. En virtud del principio de buena fe, las autoridades y los particulares presumirán el comportamiento leal y fiel de unos y otros en el ejercicio de sus competencias, derechos y deberes.
(...)
11. En virtud del principio de eficacia, las autoridades buscarán que los procedimientos logren su finalidad y, para el efecto, removerán de oficio los obstáculos puramente formales, evitarán decisiones inhibitorias, dilaciones o retardos y sanearán, de acuerdo con este Código las irregularidades procedimentales que se presenten, en procura de la efectividad del derecho material objeto de la actuación administrativa.
(...)
13. En virtud del principio de celeridad, las autoridades impulsarán oficiosamente los procedimientos, e incentivarán el uso de las tecnologías de la información y las comunicaciones, a efectos de que los procedimientos se adelanten con diligencia, dentro de los términos legales y sin dilaciones injustificadas.
Que, el Decreto número 019 de 2012, modificado por el Decreto Ley 2106 de 2019 "Por el cual se dictan normas para simplificar, suprimir y reformar trámites, procesos y procedimientos innecesarios existentes en la administración pública", señaló en su artículo 1 que esta normativa tiene por objeto: "simplificar, suprimir y reformar trámites, procesos y procedimientos innecesarios existentes en la Administración Pública bajo los principios constitucionales y legales que rigen la función pública, con el propósito de garantizar la efectividad de los principios, derechos y deberes de las personas consagrados en la Constitución mediante trámites, procesos y procedimientos administrativos sencillos, ágiles, coordinados, modernos y digitales".
Que, la Ley 2294 de 2023 "Por el cual se expide el Plan Nacional de Desarrollo 2022- 2026 Colombia potencia mundial de la vida", en su artículo 161 estableció medidas de FORTALECIMIENTO PARA AGILIZAR LAS AUTORIZACIONES DE LOS PROCESOS DE FABRICACIÓN, VENTA E IMPORTACIÓN DE MEDICAMENTOS Y DISPOSITIVOS Y TECNOLOGÍAS EN SALUD. El Ministerio de Salud y Protección Social, en articulación con el Ministerio de Ciencia, Tecnología e Innovación, adoptará las decisiones necesarias para fortalecer e incrementar la capacidad de fabricación, semielaboración, venta, importación de medicamentos, vacunas, dispositivos y otras tecnologías en salud en condiciones de calidad, seguridad, eficacia, acceso a medicamentos y competiti vidad.
Estas medidas incluirán, aunque no estarán limitadas a las siguientes:
1. Agilizar y priorizar la evaluación y certificación de Buenas Prácticas de Manufactura, y demás certificaciones que sean requeridas, para la instalación de nuevas plantas de producción en el país, así como para la ampliación y/o adecuación de las existentes.
2. Dar prioridad y reducir los tiempos aplicados a las solicitudes de trámites relacionados con los registros sanitarios correspondientes a las modalidades de fabricar y vender, importar, semielaborar y vender y de importar y vender.
3. Agilizar la entrada al mercado de medicamentos competidores (de marca o genéricos) en todos los segmentos farmacéuticos. Para esto, el Ministerio de Salud y Protección Social asegurará que se incrementen las capacidades del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima) y se puedan establecer las siguientes modificaciones:
a) Todos los trámites relacionados con evaluaciones farmacéuticas y legales de los medicamentos sean realizados por dependencias internas del INVIMA bajo criterios de idoneidad técnica y eficiencia, y no requieran conceptos previos de la Comisión Revisora. En el mismo sentido, a la Comisión Revisora solo le corresponderá emitir conceptos sobre la evaluación farmacológica de medicamentos nuevos, y en relación con aquellos temas o elementos que les sean asignados conforme al Reglamento.
b) En el caso de aquellos medicamentos competidores (de marca o genéricos) que, de acuerdo con los criterios y listados de principios activos definidos por el Ministerio de Salud, requieran en la evaluación farmacéutica de estudios de bioequivalencia y/o biodisponibilidad, la aprobación de tales estudios será realizada por una dependencia técnica interna del Invima en un plazo inferior a 3 meses.
(...)
d) Se identifiquen aquellos medicamentos correspondientes a terapias de alto costo y para enfermedades huérfanas, así como aquellos en riesgo de situación de desabastecimiento, en los que por razones de salud pública y/o de seguridad sanitaria sea necesario mantener o ampliar la producción en Colombia, para que se dé prioridad a todos los trámites relacionados con sus registros sanitarios, en las modalidades de fabricar y vender, importar, semielaborar y vender y de importar y vender. (Subrayado fuera de texto)
Que, de conformidad a la Resolución número 1229 de 2013 "Por la cual se establece el modelo de inspección, vigilancia y control sanitario para los productos de uso y consumo humano", se estableció el modelo de inspección, vigilancia y control sanitario que permite contar con un marco de referencia donde se incorpore el análisis y gestión de riesgos asociados al uso y consumo de bienes y servicios, a lo largo de todas las fases de las cadenas productivas, con el fin de proteger la salud humana individual y colectiva en un contexto de seguridad sanitaria nacional.
En este mismo sentido, el artículo 102 del Decreto número 677 de 1995, en mención establece que los titulares de los registros sanitarios son los responsables de la información suministrada sobre el medicamento, incluyendo sus indicaciones, las cuales quedarán amparadas en el registro otorgado por el Invima:
"Artículo 102. De la responsabilidad. Los titulares de licencias de funcionamiento y registros sanitarios otorgados conforme al procedimiento previsto en el presente Decreto serán responsables de la veracidad de la información suministrada y del cumplimiento de las normas sanitarias bajo las cuales fue expedido el acto administrativo que los otorga. El fabricante y el titular del registro sanitario deberán cumplir en todo momento las normas técnico-sanitarias, así como las condiciones de fabricación y de control de calidad exigidas, y es bajo este supuesto que el Invima expide la correspondiente licencia o registro. En consecuencia, los efectos adversos que sobre la salud individual o colectiva pueda experimentar la población usuaria de los productos, por transgresión de las normas y/o condiciones establecidas, será responsabilidad de los fabricantes y titular es de los registros sanitarios".
Que, el artículo 5o del Decreto número 334 de 2022, establece las clases de modificaciones al registro sanitario de medicamentos de síntesis química, gases medicinales, biológicos y homeopáticos, de acuerdo con el nivel de riesgo e impacto sobre el producto; así mismo, el artículo 8o del referido Decreto consagra el procedimiento para tramitar las solicitudes de modificaciones al registro sanitario.
Que, en virtud del artículo 5o del Decreto número 1474 de 2023, dispone que la vigencia de los registros sanitarios de medicamentos será indefinida. Aunque ello no impide que el Invima o la autoridad correspondiente, en ejercicio de las funciones de inspección, vigilancia y control, adopte las medidas necesarias al encontrar un incumplimiento de las normas técnicas que regulan la materia o identificar que existe un riesgo sanitario asociado a la farmacovigilancia durante el uso del medicamento.
Que, en el artículo 1o de la Resolución número 1411 de 2022 "Por la cual se adopta la Política de Soberanía en la producción para la Seguridad Sanitaria", señala que: "La política de soberanía en la producción para la seguridad sanitaria establece el conjunto de actividades que permiten desarrollar y robustecer la capacidad del país para producir y satisfacer las necesidades de tecnologías de salud estratégicas, fortaleciendo así las capacidades para hacer frente a situaciones de emergencia e incidentes agudos que vulneren la salud de la población".
Que, desde la vigencia 2012, fecha del último rediseño del Instituto, se han expedido 196 normas jurídicas nuevas que han impactado en las competencias, funciones y la capacidad operativa del Invima, sin contar con el respectivo respaldo presupuestal ni humano; así mismo, con ocasión a las nuevas competencias exclusivas de Inspección, Vigilancia y Control (IVC), en plantas de beneficio y fabricación de alimentos que se designaron a la Entidad, se logró la ampliación de la planta de personal del Instituto a 1.500 cargos, los cuales a la fecha no se encuentran suplidos en su totalidad por deficiencia de presupuesto, tampoco resultan ser suficientes para el cabal cumplimiento de competencias a cargo del Instituto.
Que, tanto las funciones como la estructura del Invima fueron previstas previo a la expedición del modelo de inspección, vigilancia y control sanitario para los productos de uso y consumo humano establecido por el Ministerio de Salud y Protección Social en el año 2013, siendo necesaria a la fecha una modificación estructural y actualización normativa que materialice el enfoque de riesgo en los trámites y servicios a cargo del instituto.
Que, el Instituto Nacional de Vigilancia de Alimentos y Medicamentos (Invima), ha sido víctima de varios ataques cibernéticos, afectando significativamente sus operaciones y servicios, causando una suspensión de actividades que se prolongó por varios días. En respuesta a estas circunstancias, el Instituto expidió la Resolución número 2022600000 de 2022 "Por medio de la cual se adoptan medidas administrativas transitorias necesarias para garantizar la continuidad en la prestación de los servicios y trámites a cargo del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima)", en donde se adoptó temporalmente medidas urgentes para mitigar los riesgos y suspendió los términos de los trámites que adelantaba el Instituto.
Por todo lo expuesto anteriormente, el Invima, afronta dificultades administrativas que inciden en los tiempos de respuesta a los diferentes trámites presentados ante el Instituto, es así que, se debe implementar un Plan de Contingencia que permita gestionar las solicitudes de registros sanitarios y trámites asociados.
Que, acorde al Plan de Contingencia y Conforme al Decreto número 2079 de 2012, la Dirección de Medicamentos y Productos Biológicos del Instituto, denota la necesidad de efectuar, por parte del Grupo de Talento Humano de la Secretaría General, las reubicaciones de funcionarios que correspondan.
Que, el Tribunal Administrativo de Cundinamarca Sección Primera "Subsección A", mediante sentencia de primera instancia de 12 de diciembre de 2024, dentro del Medio de Protección de los Derechos e Intereses Colectivos número 25000234100020190076300, ordenó al Instituto, lo siguiente:
v) planteamiento de soluciones concretas para poner freno a la problemática del desabastecimiento de medicamentos, en ese sentido se deberá estudiar el fortalecimiento del Invima en cuanto al personal técnico y herramientas que permitan expedir los registros sanitarios en el menor tiempo posible.
(...)
2.2 ORDENAR al Ministerio de Salud y Protección Social y al Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima), que continúe ejecutando el Plan de Respuesta Urgente a la crisis de desabastecimiento de medicamentos e insumos.
Que, la Circular DG 1000-0012-2023, estableció los criterios para priorizar las solicitudes de registro sanitario y trámites asociados que se les aplica la gestión preventiva del riesgo de desabastecimiento de medicamentos.
Que, al 30 de diciembre de 2024, se encontraban en trámite un total de 14.549 solicitudes de registros sanitarios y trámites asociados pendientes por resolver.
Que, de acuerdo con lo expuesto, la Dirección General y la Dirección de Medicamentos y Productos Biológicos del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima), en aras de dar respuesta a los trámites radicados ante el Instituto y garantizar la seguridad sanitaria en los medicamentos y productos biológicos en el país, denota la necesidad de establecer y adoptar un Plan de Contingencia que le permita al Instituto, evaluar de manera eficiente, agilizando las decisiones que corresponda y en consecuencia las actuaciones administrativas se cumplan en el menor tiempo posible.
Que, en mérito de lo expuesto,
RESUELVE:
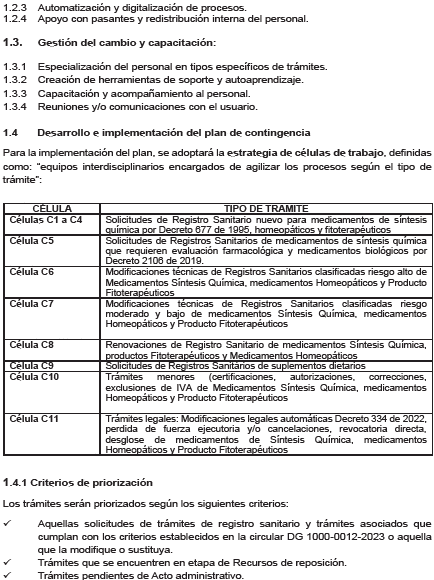
ARTÍCULO 1o. OBJETO. Adoptar el Plan de Contingencia para la racionalización y reforzamiento de las capacidades estructurales y procedimentales en la expedición y modificaciones de Registros Sanitarios y trámites asociados a cargo de la Dirección de Medicamentos y Productos Biológicos del Instituto Nacional de Vigilancia de Medicamentos y Alimentos (Invima), contenido en el Anexo Técnico "Plan de Contingencia", el cual hace parte integral del presente acto administrativo.
ARTÍCULO 2o. CLASIFICACIÓN ENFOQUE DE RIESGO SANITARIO. La Dirección de Medicamentos y Productos Biológicos del Invima, tramitará y resolverá las solicitudes de los registros sanitarios y trámites asociados, que se clasifican y detallan en el Anexo Técnico "Plan de Contingencia", según el enfoque y gestión preventiva del riesgo.
ARTÍCULO 3o. USO DE TECNOLOGÍAS EN LOS PROCEDIMIENTOS. La Dirección de Medicamentos y Productos Biológicos, hará uso de las tecnologías de la información y las comunicaciones en sus procedimientos, así:
1. Realización de reuniones y/o comunicaciones con los solicitantes y/o titulares de los trámites de registros sanitarios y trámites asociados, con el fin de subsanar, aclarar y complementar la información que se requiera dentro del término establecido en la norma aplicable, para la pronta adopción de decisiones. Las reuniones se podrán realizar de manera presencial, en cualquier caso, se dejará constancia de su desarrollo, compromisos y conclusiones en acta.
De forma previa con la citación a la reunión, el Invima, comunicará al administrado las inquietudes que surjan dentro del trámite, para que el interesado pueda preparar la sesión de revisión.
2. En los trámites de expedición o modificación de registros, certificados y de productos vitales no disponibles, en los cuales contemple la presentación de documentos de carácter público expedidos en el extranjero, tales como certificado de Buenas Prácticas, Certificado de Condiciones de Fabricación, Certificados de Capacidad de Producción, Certificado de Venta Libre o certificaciones equivalentes, el Invima consultará en la página web oficial de las autoridades competentes la información pertinente para verificar la información. Para tal efecto, el interesado deberá indicar el enlace web respectivo y deberá allegarlo a través del medio que se comunique par a tal fin.
El Invima, adoptará la decisión con base en la verificación en la página web oficial de las autoridades competentes.
ARTÍCULO 4o. GESTIÓN DEL RIESGO DE DESABASTECIMIENTO DE MEDICAMENTOS Y CASOS POR GESTIÓN PREVENTIVA DEL RIESGO. La Dirección de Medicamentos y Productos Biológicos, para los casos de la gestión preventiva del riesgo de desabastecimiento tendrá en cuenta las siguientes condiciones de priorización:
1. MEDICAMENTOS DECLARADOS EN DESABASTECIMIENTO O EN RIESGO DE DESABASTECIMIENTO: Para que un producto aplique a esta categoría, debe estar incluido en el listado vigente de medicamentos declarados en desabastecimiento o en riesgo de desabastecimiento por el Invima, de conformidad con lo establecido en la Circular DG 1000-0012- 2023, o aquella que la modifique o sustituya.
Nota: No aplicará la priorización para los medicamentos que figuran en el listado con el estado de monitorización y no desabastecidos y aquellos cuyo registro se encuentra en estado suspendido.
2. MEDICAMENTOS ESTRATÉGICOS EN SALUD PÚBLICA. Aplica para aquellos medicamentos incluidos por el Ministerio de Salud y Protección Social, en negociaciones o compras centralizadas, los declarados de interés público y los estratégicos para atender los programas de salud pública.
En este caso debe existir una solicitud expresa de la Dirección de Medicamentos y Tecnologías del Ministerio de Salud y Protección Social a la Dirección de Medicamentos y Productos Biológicos del Invima.
3. CAMBIO DE PLANTAS FARMACÉUTICAS NUEVAS POR CUMPLIMIENTO DEL INFORME 37 Y 45: Las solicitudes de modificaciones a los registros sanitarios derivada de cambio/traslado de las plantas farmacéuticas nuevas en Colombia por cumplimiento de las buenas prácticas de manufactura del informe 37 y 45, se gestionarán de conformidad con el riesgo sanitario que se determine.
4. SOLICITUDES DE REGISTROS SANITARIOS DE GASES MEDICINALES: Aplica aquellas solicitudes de registros sanitarios que se encuentran en el marco del Plan de Contingencia.
5. TRÁMITES ASOCIADOS AL REGISTRO SANITARIO: Para estos casos se aplicarán los criterios establecidos en la Circular DG1000-0012- 2023, o aquella que la modifique o sustituya.
6. <Numeral adicionado por el artículo 1 de la Resolución 2025046281 de 19 de septiembre de 2025> Adición o Sustitución de Fabricante por seguimiento a temas de desabastecimiento, sobre la evaluación y análisis de la situación específica por parte de la Dirección de Medicamentos y Productos Biológicos.
7. <Numeral adicionado por el artículo 1 de la Resolución 2025046281 de 19 de septiembre de 2025> Solicitud de registro sanitario nuevo y modificaciones de vacunas que se encuentren asociadas a la prevención de enfermedades respiratorias agudas.
PARÁGRAFO. Todas las solicitudes de registro sanitario y trámites asociados que requieran estudios de biodisponibilidad y/o bioequivalencias, radicadas antes de la entrada en vigencia de la Ley 2294 de 2023 y que se encuentren en curso, serán estudiadas por el Grupo de Registros Sanitarios de la Dirección de Medicamentos y Productos Biológicos, sin que se requiera un concepto por parte de la Sala Especializada de Medicamentos de la Comisión Revisora.
PARÁGRAFO 2o. <Parágrafo adicionado por el artículo 1 de la Resolución 2025046281 de 19 de septiembre de 2025> La evaluación de los trámites radicados bajo tarifa 4049-2(Estudios de Biodisponibilidad y Bioequivalencia), acogerá el derecho al turno de la solicitud del trámite de Registro Sanitario nuevo.
ARTÍCULO 5o. MESA TÉCNICA DE SEGUIMIENTO, EVALUACIÓN Y VERIFICACIÓN. Se constituirá una Mesa Técnica de seguimiento, evaluación y verificación la cual estará conformado por:
1. El Director (a) General o su delegado.
2. La Directora de Medicamentos y Productos Biológicos o su asignado.
3. El Jefe (a) de la Oficina de Tecnologías de la Información o su asignado.
4. El Jefe (a) de la Oficina Asesora Jurídica o su asignado.
5. El Jefe (a) de la Oficina de Control Interno.
6. Director (a) de Medicamentos y Tecnologías en Salud del Ministerio de Salud y Protección Social o su asignado (en calidad de invitado).
PARÁGRAFO 1o. La Mesa Técnica de que trata el presente artículo, se reunirá de manera quincenal, con el fin de realizar el seguimiento, evaluación y verificación de la ejecución del Plan de Contingencia adoptado por el presente acto administrativo.
PARÁGRAFO 2o. Los resultados y gestiones adelantadas en el marco del Plan de Contingencia serán presentadas por parte de la Dirección de Medicamentos y Productos Biológicos de manera mensual en el Comité Institucional de Gestión y Desempeño de la Entidad, de acuerdo con la estructura definida por la Secretaria Técnica del Comité con el Apoyo de la Oficina Asesora Jurídica.
ARTÍCULO 6o. ARCHIVO DE TRÁMITES POR CIBERATAQUES. La Dirección de Medicamentos y Productos Biológicos del Instituto, previo agotamiento de la comunicación por diez (10) días a los interesados, podrá realizar el archivo de las solicitudes de trámite de registro sanitario presentadas en el tiempo de los ataques cibernéticos del año 2022 y que fueron cifradas, lo que hace imposible su recuperación.
PARÁGRAFO. Los interesados en continuar con los trámites deberán allegar al Instituto la documentación que haga parte del trámite, con el fin de dar continuidad a este. Este trámite no generará costo.
Los radicados que sean requeridos mediante correo electrónico o de cualquier otro medio tecnológico institucional dispuesto, serán objeto de publicación en la página Web del Instituto.
ARTÍCULO 7o. RECURSOS TÉCNICOS. La Oficina de Tecnología de la Información del Instituto, dispondrá de los recursos técnicos existentes para el apoyo y desarrollo del Plan de Contingencia establecido por la Dirección de Medicamentos y Productos Biológico y adoptado por medio del presente acto administrativo.
ARTÍCULO 8o. REUBICACIÓN. La Dirección de Medicamentos y Productos Biológicos, solicitará al Grupo de Talento Humano de la Secretaria General del Instituto, la reubicación del empleo de los funcionarios necesarios para la ejecución del Plan de Contingencia adoptado por medio de esta Resolución, para lo cual, se efectuarán las respectivas revisiones del manual específico de funciones y competencias laborales que apliquen, garantizando el cumplimiento de los requisitos mínimos de acuerdo con la norma que rija la materia.
ARTÍCULO 9o. TÉRMINO DE EJECUCIÓN. El Plan de Contingencia aquí previsto tendrá una vigencia de seis (06) meses.
ARTÍCULO 10. VIGENCIA Y DEROGATORIA. La presente resolución rige a partir de la fecha de su publicación en el Diario Oficial y deroga las disposiciones que le sean contrarias.
Publíquese, comuníquese y cúmplase.
Se expide en Bogotá, D. C., a 19 de marzo de 2025.
El Director General,
Francisco A. G. Rossi Buenaventura.
La Directora Técnica de Medicamentos y Productos Biológicos,
Sandra María Montoya Escobar