RESOLUCIÓN 1333 DE 2010
Gaceta Oficial No. 1848 de 2 de julio de 2010
SECRETARÍA GENERAL DE LA COMUNIDAD ANDINA
<NOTA DE VIGENCIA: Resolución derogada a partir del 1 de marzo de 2021 por la Resolución 2108 de 2019, la cual entrará en vigencia conjuntamente con la Decisión 833>
Adiciones a la Resolución 797 – Criterios de homologación de la codificación en materia de cosméticos. Formatos para la Notificación Sanitaria Obligatoria (NSO) de productos cosméticos, su renovación, reconocimiento y cambios.
LA SECRETARÍA GENERAL DE LA COMUNIDAD ANDINA,
VISTOS: Los artículos 5, 7, 8, 11, 12, 14, 15, 23, 30, la Disposición Transitoria única de la Decisión 516 y los Capítulos II y VIII de la Resolución 797;
CONSIDERANDO:
Que la Decisión 516 señala que los productos cosméticos requieren de la Notificación Sanitaria Obligatoria (NSO) para su comercialización o expendio en la Subregión y establece los requisitos que deberán acompañar a la Notificación Sanitaria Obligatoria y la solicitud de reconocimiento del código de identificación asignado por la Autoridad Nacional Competente para facilitar el etiquetado, la vigilancia y el control sanitario;
Que la misma Decisión señala que los interesados deberán informar debida e inmediatamente a la Autoridad Nacional Competente los cambios a la Notificación Sanitaria Obligatoria, adjuntando la documentación respectiva;
Que de acuerdo con el literal c) del artículo 30 de la Decisión 516 y el artículo 20 de la Resolución 797 los Países Miembros, a través de sus respectivas Autoridades Nacionales Competentes, se prestarán asistencia mutua y cooperación e intercambiarán información para la implementación de un Sistema de Información que ayude a prevenir, investigar y combatir los riesgos sanitarios de cosméticos;
Que para la implementación de un Sistema de Información resulta necesario armonizar los formatos para la Notificación Sanitaria Obligatoria, de reconocimiento y renovación del código de identificación de la NSO, información de cambios así como los formatos de respuesta de la Autoridad Nacional Competente en la que asigne y reconozca el código de identificación de NSO;
Que también es necesario contar con una estructura armonizada del código de identificación de la NSO entre los Países Miembros, a fin de que se facilite su reconocimiento, control y vigilancia;
Que de acuerdo con lo previsto en la Decisión 516 la Secretaría General, previa consulta a las Autoridades Nacionales Competentes en materia de cosméticos, adoptó mediante Resolución 797 el Reglamento sobre Control y Vigilancia Sanitaria;
Que, para completar los criterios de homologación de la codificación en dicha materia, es necesario adicionar al referido reglamento la delimitación de la responsabilidad de los químicos farmacéuticos y los formatos para la Notificación Sanitaria Obligatoria, así como para su renovación, reconocimiento y cambios;
Que, las Autoridades Nacionales Competentes en materia de cosméticos, en su reunión celebrada el 25 de mayo de 2010 manifestaron su conformidad en relación con el contenido del Proyecto de Resolución que adiciona a la Resolución 797 la participación y responsabilidad de los químicos farmacéuticos y adopta los formatos para la Notificación Sanitaria Obligatoria, la solicitud de renovación y reconocimiento del Código de identificación de la NSO, la información de cambios y la estructura de codificación de la NSO para productos cosméticos;
RESUELVE:
ARTÍCULO 1o.- <Resolución derogada a partir del 1 de marzo de 2021 por la Resolución 2108 de 2019, la cual entrará en vigencia conjuntamente con la Decisión 833> Añadir al artículo 2 de la Resolución 797 el siguiente párrafo:
“La información sobre el producto, que se suministre a las Autoridades Nacionales Competentes o que sea solicitada por alguna de ellas, deberá contar con el respaldo de un químico farmacéutico titulado y colegiado, que sea el responsable de la Dirección Técnica de la empresa, según lo previsto en el numeral 3, título II del Anexo 2 de la Decisión 516, quien certificará técnicamente las condiciones de calidad del producto cosmético. La responsabilidad del químico farmacéutico estará limitada al alcance de la certificación que en su ejercicio profesional emita.”
ARTÍCULO 2o.- <Resolución derogada a partir del 1 de marzo de 2021 por la Resolución 2108 de 2019, la cual entrará en vigencia conjuntamente con la Decisión 833> Incorporar a continuación del artículo 22 de la Resolución 797 los siguientes artículos:
“Artículo 23.- Adoptar los formatos FNSOC-001, FNSOC-002 y FNSOC-003 y su instructivo de aplicación indicados en los Anexos I y II de la presente Resolución, para que sean aplicados por los interesados y las Autoridades Nacionales Competentes (ANC), cuando los primeros presenten notificaciones sanitarias obligatorias, solicitudes de reconocimiento, renovaciones del código de identificación e información sobre cambios de la NSO, y las ANC tengan que dar respuesta a los interesados sobre las notificaciones sanitarias obligatorias, las solicitudes de reconocimiento y las renovaciones, de acuerdo con lo previsto en la normativa andina sobre la materia.”
“Artículo 24.- Adoptar la estructura armonizada del código de identificación de la NSO indicada en el Anexo III, que aplicarán las Autoridades Nacionales Competentes para coordinar sus acciones de control y vigilancia en materia de productos cosméticos.”
ARTÍCULO 3o.- La presente Resolución entrará en vigencia a partir de su publicación en la Gaceta Oficial del Acuerdo de Cartagena.
Dada en la ciudad de Lima, Perú, a los treinta días del mes de junio del año dos mil diez.
ADALID CONTRERAS BASPINEIRO
Secretario General a.i.
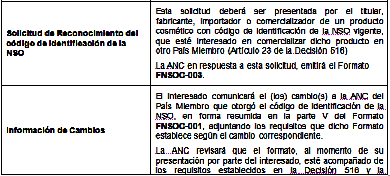
INSTRUCTIVO PARA EL LLENADO DEL FORMATO FNSOC-001
El objeto del formato FNSOC-001 será definido por el interesado en calidad de Declaración Jurada y lo hará de conocimiento de la Autoridad Nacional Competente (ANC) colocando una “X”, según sea el caso.
Los demás campos del Formato FNSOC-001 serán llenados obligatoriamente, independientemente del objeto del formato, salvo indicación en contrario registrada en el propio campo.
En todo momento, el interesado deberá regirse por lo establecido en la Decisión 516 y/o la Resolución 797 señalados en los campos del Formato FNSOC-001.




![]()

![]()



![]()



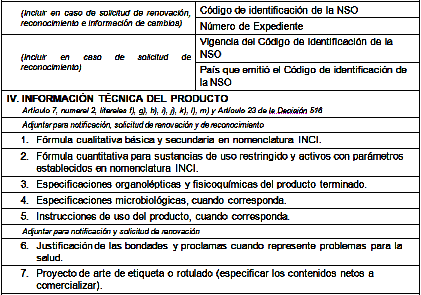
VII. CERTIFICACIÓN DE LA INFORMACIÓN TÉCNICA DEL PRODUCTO
Yo, ____________________________________________, identificado con ______________, actuando en mi condición de químico farmacéutico titulado y con registro profesional No. ________ de (País Miembro correspondiente) certifico técnicamente que el producto cosmético descrito no perjudica la salud humana, siempre que se apliquen las condiciones normales o razonablemente previsibles de uso.
FIRMA DEL RESPONSABLE TÉCNICO (QUÍMICO FARMACÉUTICO)
Nombre completo:
Número de Registro o Colegiatura Profesional:
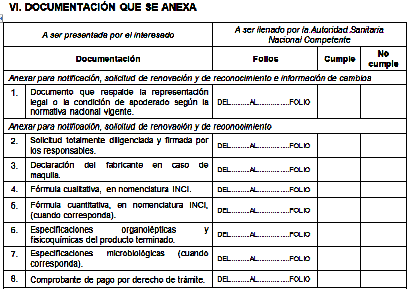
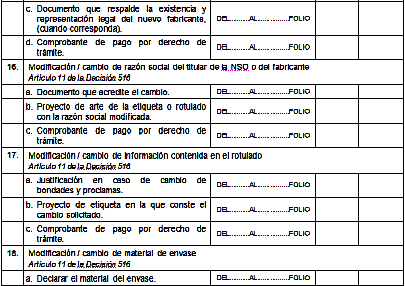
VIII. DECLARACION JURADA.
Yo, __________________________________________, identificado con ________________, actuando en condición de Representante legal o Apoderado, declaro bajo la gravedad de juramento, que el presente documento y la información suministrada adjunta son auténticos y veraces, y cumplen con todos los requisitos establecidos por la Decisión 516 de Comisión de la Comunidad Andina y la Resolución 797 de la Secretaría General de la Comunidad Andina. Asimismo, declaro que la comercialización será posterior a la presentación del presente documento cumpliendo estrictamente con las especificaciones de calidad definidas para el producto.
FIRMA DEL REPRESENTANTE LEGAL O APODERADO
Nombre completo:
Número de identificación:
Lugar y fecha,
FORMATO FNSOC-002


De igual manera, este (a) (nombre Autoridad Sanitaria correspondiente), manifiesta que el interesado declaró bajo la gravedad de juramento, que el producto notificado cumple con todos los requisitos establecidos por la Decisión 516 de la Comisión de la Comunidad Andina, que toda la información suministrada a la autoridad es auténtica y veraz, que su comercialización será posterior a la notificación, cumpliendo estrictamente con las especificaciones de calidad definidas para el producto y que se encuentra sometido al control y vigilancia posterior por parte de las Autoridades Sanitarias correspondientes, de acuerdo con lo establecido en la referida Decisión 516 y la Resolución 797 de la Secretaría General de la Comunidad Andina, por lo tanto asume la responsabilidad sobre cualquier inconsistencia que se presente entre la información suministrada y la que resulte de las acciones que se ejerzan por parte de las autoridades.
_____________________________________________
FIRMA DE LA AUTORIDAD SANITARIA
Lugar y fecha,


Asimismo, este (a) (nombre Autoridad Sanitaria correspondiente), manifiesta que el interesado declaró bajo la gravedad de juramento, que el producto notificado cumple con todos los requisitos establecidos por la Decisión 516 de la Comisión de la Comunidad Andina, que toda la información suministrada a la autoridad es auténtica y veraz, que su comercialización será posterior a la fecha en que el interesado solicita el reconocimiento, cumpliendo estrictamente con las especificaciones de calidad definidas para el producto y que se encuentra sometido al control y vigilancia posterior por parte de las Autoridades Sanitarias correspondientes, de acuerdo con lo establecido en la referida Decisión y la Resolución 797 de la Secretaría General de la Comunidad Andina, por lo tanto asume la responsabilidad sobre cualquier inconsistencia que se presente entre la información suministrada y la que resulte de las acciones que se ejerzan por parte de las autoridades.
De acuerdo a lo establecido en el artículo 18 de la Decisión 516 y al artículo 2 de la Resolución 797, el titular o representante legal deberá presentar la etiqueta del producto cuya NSO ha sido reconocida, antes de iniciar su comercialización.
_____________________________________________
FIRMA DE LA AUTORIDAD SANITARIA
Lugar y fecha,
CÓDIGO DE IDENTIFICACIÓN NSO PARA PRODUCTOS COSMÉTICOS
Los países acordaron la siguiente estructura del código de la NSO con la inclusión de los siguientes campos:
(cinco dígitos) (dos últimos dígitos)
Las Autoridades Sanitarias Nacionales Competentes tendrán potestad para incluir al final de la estructura de la codificación de identificación NSO, otros campos que sean de utilidad para el control y vigilancia en el mercado siempre que guarde concordancia y no contradiga lo previsto en la Decisión 516 de la Comisión de la Comunidad Andina y la Resolución 797 de la Secretaría General de la Comunidad Andina.
* * * *







